固有免疫应答是宿主识别与抵抗病原体感染的第一道防线,对激活适应性免疫进而清除病原体至关重要。位于细胞膜表面、内体或细胞质的模式识别受体(pattern recognition receptor,PRRs)通过识别病原体相关分子模式(pathogen-associated molecular patterns,PAMPs)或宿主损伤相关分子模式(damageassociated molecular patterns,DAMPs)启动固有免疫应答抑制病原体的感染。作为固有免疫的重要组成部分,细胞焦亡是一种由 Gasdermin (GSDM)家族蛋白活化介导的新型程序性细胞死亡,在清除内源病变或外源感染过程中发挥关键作用。
什么是细胞焦亡
细胞焦亡是一种由Gasdermin家族蛋白介导的新型程序性细胞死亡。当宿主细胞感应病原体感染或其他危险信号时,Gasdermin 家族蛋白被切割活化并诱导细胞焦亡。细胞焦亡过程往往伴随大量炎性细胞因子释放,这些炎性细胞因子在宿主清除病原体过程中发挥着至关重要作用。
关键蛋白Gasdermin
Gasdermin家族包含六个成员: GSDMA 、GSDMB、GSDMC、GSDMD、GSDME(又称 DFNA5)
和PJVK(又称 DFNB59)。除PJVK外,GSDMA-E均由功能保守的N端结构域(GSDM-NT)和C端结构域(GSDM-CT)组成。GSDM-NT能够结合细胞膜酸性磷脂或线粒体心磷脂,并在膜上多聚化形成孔洞以诱导细胞焦亡。大量研究结果显示革兰氏阴性菌主要通过激活炎症小体(inflammasome)进而切割活化GSDMD以触发细胞焦亡。
炎症小体包括经典炎症小体和费经典炎症小体。经典炎症小体主要由Caspase-1、胞质内的
模式识别受体(NLRP3、NLRC4、NLRP1、AIM2、Pyrin等)和凋亡相关斑点样蛋白(Apoptosis-associated Speck-like Protein,ASC)组成。经典炎症小体组装后激活Caspase-1进而切割GSDMD,释放GSDMD-NT导致细胞焦亡。与此同时,Caspase-1切割活化IL-1β和白介素18(IL-18)等促炎症因子,招募免疫细胞,清除外源病原体或内源病变。
非经典炎症小体由病原菌感染条件下释放脂多糖(lipopolysaccharide,LPS)至胞内直接结合并激活Caspase-4/5/11,活化的Caspase-4/5/11切割 GSDMD形成具有成孔活性的GSDMD-N 端结构域并诱导细胞焦亡。
近年来,不依赖于炎症小体介导的细胞焦亡通路的活化机制相继报道。包括,细胞凋亡通路的执行蛋白Caspase-3能够切割GSDME,释放GSDME-NT,促使细胞凋亡转变为细胞焦亡;GSDMD 能够被中性粒细胞弹性蛋白酶(neutrophil elastase,ELANE)和组织蛋白酶G(cathepsin G,CatG)切割活化,引起细胞焦亡;杀伤细胞释放颗粒酶 B(granzyme B,GZMB)直接切割肿瘤细胞GSDME触发肿瘤细胞焦亡;耶尔森菌(Yersinia)分泌的外膜蛋白J(Yersinia outer protein J,YopJ)抑制转化生长因子β激活激酶 1 (transforming growth factor-β-activated Kinase 1,TAK1),激活RIPK1/Caspase-8复合体,活化的Caspase-8切割GSDMD导致细胞焦亡;族链球菌(Group A Streptococcus,GAS)感染过程中释放的效应蛋白链球菌热源性外毒素B (Streptococcal pyrogenic exotoxin B,SpeB),一种胱氨酸蛋白酶,直接剪切宿主GSDMA诱导细胞焦亡等等。这些研究进一步拓展和突出了细胞焦亡在抗感染和抗肿瘤领域的功能。
病原体抑制细胞焦亡的新策略
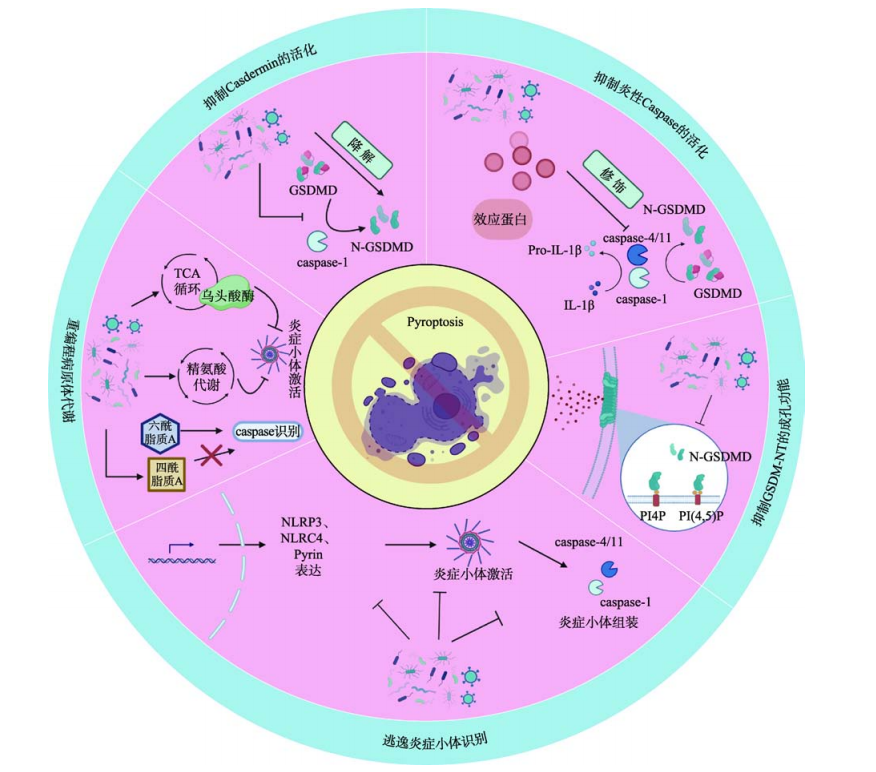
Novel strategies for pyroptosis suppression by pathogen
病原体在与宿主长期“博弈”过程中进化出多种抑制细胞焦亡的策略,主要包括:
(1) 逃逸炎症小体识别;
病原体可从抑制模式识别受体激活和表达、抑制炎症小体组装等方面逃逸宿主炎症小体识别。干扰宿主炎症小体对病原体的识别已经成为细菌发生免疫逃逸的新策略,对于增强细菌的毒力并建立有效的感染至关重要。
(2) 重编程病原体自身代谢抑制炎症小体活化;
巨噬细胞 (macrohages) 是免疫系统中的重要细胞,能够吞噬和消灭病原体,巨噬细胞表面的酪氨酸激酶受体VEGFR3与AMPK形成的信号轴能整合糖代谢、炎症小体活化、细胞焦亡和吞噬清除细菌的功能。
(3) 分泌效应蛋白抑制炎性 Caspase的活性;
病原体分泌的效应蛋白能够直接与Caspase相互作用并抑制其活性从而阻断炎症小体介导的细胞焦亡。
(4) 抑制Gasdermin的活化;
Gasdermin 家族蛋白是细胞焦亡的关键执行蛋白,病原体可以直接抑制该家族蛋白的活性和表达而抑制细胞焦亡。
(5) 抑制GSDM-NT的成孔功能。
泛素化是一种能够调节多种细胞功能的翻译后修饰,由活化酶E1,结合酶E2 和连接酶E3 催化完成。泛素化不仅能够靶向底物蛋白以26S蛋白酶体依赖的方式使其降解,还在调节先天性和适应性免疫反应以及免疫耐受方面具有关键作用。一些病原体已进化出复杂的机制以逃避或抵消泛素依赖的宿主反应,其中由病原体编码的 E3 泛素连接酶和去泛素化酶在病原体-宿主细胞相互作用中发挥至关重要的作用。
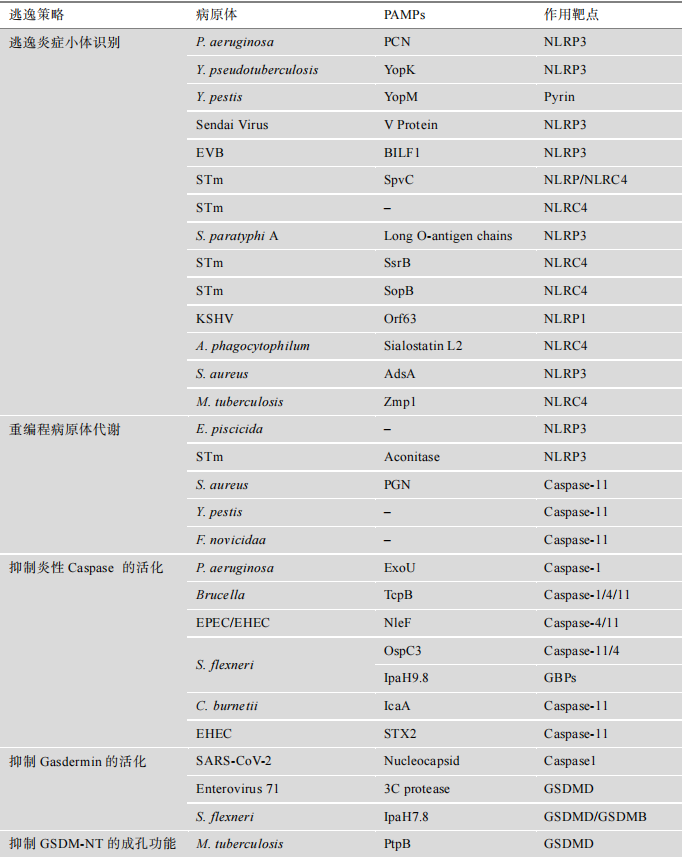
Novel strategies for pyroptosis suppression by pathogen
细胞焦亡是机体抵抗病原体感染的一种重要天然免疫反应,而病原体在宿主免疫系统的压力下进化出了适应性策略来抑制细胞焦亡以实现持续感染。病原体逃逸细胞焦亡的相关研究有助于进一步了解病原体-宿主相互作用机制,为开发新型抗感染治疗策略奠定了重要理论基础。

 联系我们
联系我们





