自身免疫疾病(autoimmune diseases,AID)是指机体对正常组织发生异常免疫反应,导致自身抗体过度产生,这些自身抗体会攻击机体自身的细胞、组织、器官,引起炎症反应,最终对机体造成损害的一类慢性系统性疾病。根据免疫反应发生的部位可以分为系统性自身免疫病和器官特异性自身免疫病两类。其中系统性自身免疫病包括:系统性红斑狼疮(systemic lupus erythematosus,SLE)、类风湿性关节炎(rheumatoidarthritis,RA)、原发性干燥综合征(primary Sjogren syndrome,SS);器官特异性自身免疫病包括:Ⅰ型糖尿病(type 1 diabetes,T1D)、特发性膜性肾病(idiopathic membranous nephropathy,IMN)、多发性硬化症(multiple sclerosis,MS)、重症肌无力(myasthenia gravis,MG)、扩张型心肌病(dilated cardiomyopathy,DCM)等30多种。
目前免疫抑制剂、单克隆抗体药物以及器官切除、血浆置换(plasma exchange,PE)等在常规自身免疫性疾病的应用较为广泛,免疫抑制剂和单克隆抗体药物虽然具有特异性,但通常需要终身免疫抑制治疗;而器官切除、血浆置换等方法伴随着各种副作用和感染风险,因此开发更有针对性的方法来应对该类疾病是相关领域一个重要的目标,针对性去除免疫系统中特定自身免疫成分的新疗法——免疫吸附(immunoadsorption,IA)成为了治疗自身免疫疾病的热门研究方向。
免疫吸附疗法是将患者血液引出后,首先通过血浆分离器将血液的血细胞成分(包括红细胞、白细胞和血小板)和血浆分开,血细胞成分输回患者体内,血浆进入吸附器,利用具有高度亲和力的吸附剂(包括具有物理化学亲和力的某些特定物质、抗原或抗体)结合特定物质,吸附后的血浆再回输至患者体内。
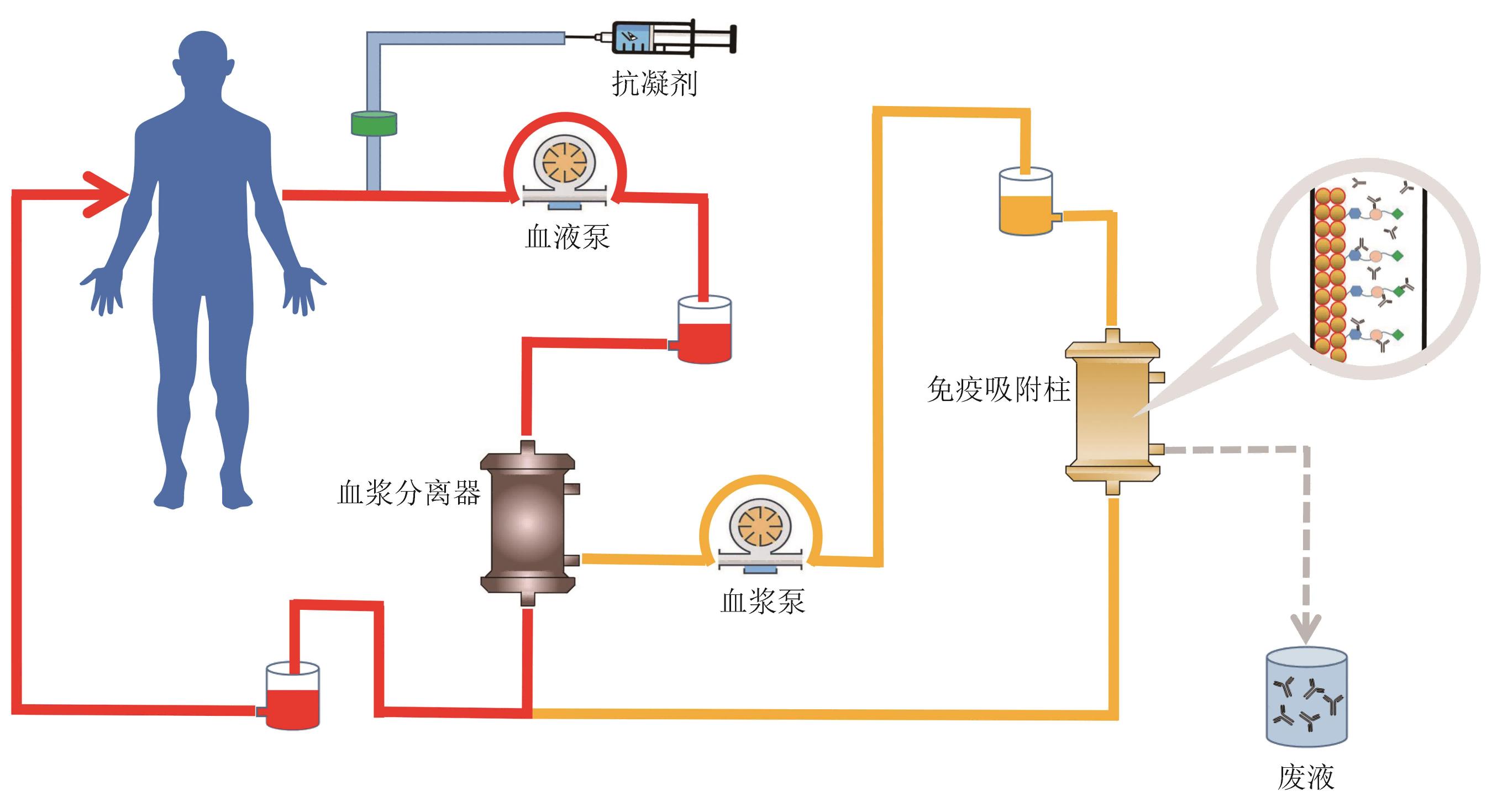
Schematic diagram of immunoadsorption therapy
免疫吸附(immunoadsorption,IA)主要是通过吸附柱的物理静电吸附或通过抗原抗体结合的原理去除血液中的致病因子,包括乙酰胆碱受体(acetylcholine receptor,AChR)、神经节苷酯抗体及N-甲基-D-天冬氨酸受体(N-methyl-D-aspartic acid receptor,NMDAR)抗体等疾病特异性的自身抗体、补体和炎症因子。
常用的免疫吸附类型包括非选择性免疫吸附(如蛋白A吸附、多克隆抗人IgG抗体吸附、色氨酸吸附等)和选择性免疫吸附。非选择性免疫吸附是指吸附剂可以结合多种非致病蛋白质或者参与自身免疫疾病的一类特定蛋白质。
蛋白A是从A型金黄色葡萄球菌细胞壁分离而得的一种分子质量约42 ku的蛋白质,其氨基末端有4个高度类同的Fc结合区,可与免疫球蛋白IgG1、IgG2和IgG4的Fc部分结合,并对IgG3、IgA、IgM和IgE有较低亲和力。此外,蛋白A还能有效与免疫复合物结合。由于蛋白A的免疫吸附对IgG不同亚类的亲和力并不相同,其对不同类型抗体吸附效果的不同。因此,蛋白A能通过非选择免疫吸附多种抗体(包括致病抗体)从而改善疾病程度。
多克隆抗人IgG抗体通过用高度纯化的人IgG抗体对动物进行免疫,然后从动物的血浆中分离出抗原特异性的抗人IgG抗体。常采用多克隆羊抗人IgG抗体共价结合制成吸附柱。由于不同免疫球蛋白类不同Fc表位之间的交叉反应性,IgG、IgA、IgM和部分IgE被吸附到绵羊抗体上,从而去除患者血浆中的Ig。
色氨酸在其分子结构上同时具有亲水性和疏水性基团,因此致病物质可通过离子和疏水相互作用吸附在色氨酸柱表面。聚乙烯醇基质上的色氨酸与IgG、IgM、IgA和一些IgE结合。色氨酸吸附后的血浆中补体成分C3、C1、C3b和C4b下降均超过50%。色氨酸柱的显著特征是免疫原性低、对IgG3亚类亲和力高、IA后感染风险最小。
选择性免疫吸附即抗体特异性免疫吸附,是将与某种特定致病抗体受体相同结构的合成肽偶联到琼脂糖柱或其他吸附柱上,通过选择性吸附特定致病抗体(例如,抗β1肾上腺素受体抗体(anti-β1-adrenoceptor antibodies,β1-AR Ab)、抗VRT-101抗体(anti-VRT-101 antibodies)和抗乙酰胆碱受体抗体(anti-AChR antibodies,AchR-Ab)等),从而改善疾病程度。
免疫吸附(immunoadsorption,IA)在自身免疫疾病中的研究
由于自身免疫疾病治疗的常规方法缺乏足够的安全性和长效性,免疫吸附在诸如扩张型心肌病、特发性膜性肾病、系统性红斑狼疮、重症肌无力等多自身免疫疾病中已开展了相关研究和临床应用。
扩张型心肌病(DCM)是一种慢性心肌疾病,其特征是与心脏扩张相关的收缩功能障碍,这是心力衰竭的常见原因,也是心脏移植的主要适应症之一。研究人员在DCM患者中发现了针对各种心脏细胞蛋白的抗体,如β1肾上腺素受体(β1-adrenoceptor, β1-AR)、线粒体蛋白、心肌肌球蛋白、毒蕈碱受体和收缩蛋白等。其中,有充分的证据表明针对β1肾上腺素受体的抗体,直接影响心功能及其病理生理学。此外,在动物中,这些自身抗体已被证明可诱导类似于人类DCM患者的心脏功能障碍。这些针对心脏蛋白的抗体主要属于IgG类,因此,针对这些自身抗体的免疫吸附治疗对DCM患者来说可能是一种很有前途的新治疗选择。
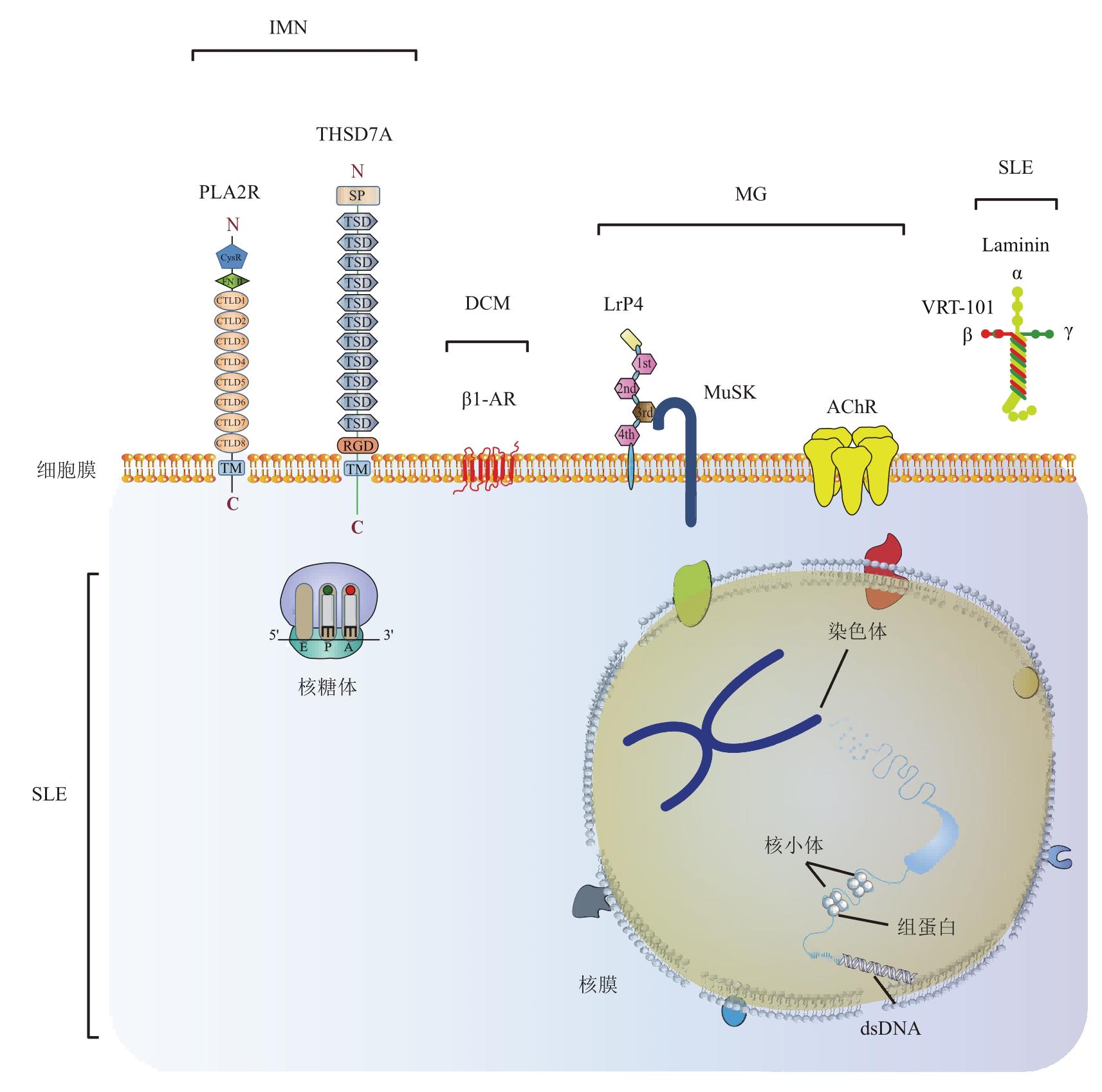
Schematic showing of autoantigens in IMN,DCM,MG and SLE
IMN是以肾小球基底膜上皮细胞下免疫复合物沉积伴基底膜弥漫性增厚为病理特点的自身免疫性疾病,是成人肾病综合征最常见的病因之一。其临床表现为蛋白尿、血尿和水肿。研究发现,70%~80%的IMN患者可检测到M型磷脂酶A2受体(PLA2R)的抗体,约有5%~10%的IMN患者中可发现Ⅰ型血小板反应蛋白7A结构域(THSD7A)抗体,并且抗足细胞PLA2R和THSD7A的肾源性自身抗体与膜性肾病相关。这两个抗体主要为IgG4亚类,但所有IgG亚类均可检测到。1999年,Esnault等首次报道免疫吸附在IMN中的治疗应用,Weinmann-Menke等使用羊抗人Ig抗体(TheraSorb-Ig)免疫吸附柱(可以去除IgG (IgG1-IgG4)、IgA、IgM、IgE和免疫复合物),表明免疫吸附可能是治疗THSD7A抗体阳性膜性肾病患者的有效方法。
SLE是一种较常见的累及多系统、多器官的自身免疫性疾病,主要以免疫系统攻击自身组织,产生大量自身抗体。自身抗体是SLE的标志,其中有些抗体是致病性的,它们直接或通过形成免疫复合物与细胞和底物结合,诱导细胞激活、炎症和组织损伤,例如抗dsDNA抗体、抗核糖体P蛋白抗体、抗核小体抗体、抗组蛋白抗体。研究已经证明,针对细胞外膜成分的狼疮抗体可与肾脏结合并造成损害,抗原目标表位是位于层黏连蛋白α链球状部分的21肽,命名为VRT-101。抗VRT-101抗体的滴度与疾病活性相关,其致病特性也在小鼠实验中得到了证实。自身抗体(主要是IgG类)是SLE主要的致病因子,因此可以通过免疫吸附治疗降低患者血浆中的致病抗体,缓解病情、减缓靶器官的损伤。
MG是一种以肌肉无力和骨骼肌疲劳为特征,针对骨骼肌神经肌肉接点(NMJ)的抗体介导的自身免疫性疾病。在大多数MG患者中(~85%),自身抗体针对肌肉乙酰胆碱受体(AChR)。AChR由5个同源亚基组成。虽然AChR有几个靶向表位,但大多数抗AChR抗体是针对主要免疫原性区(MIR),这是位于AChRα亚基上的一组重叠表位,这些亚基的核心是由氨基酸67~76形成的。参与MG的大多数抗原表位位于AChR亚基的胞外结构域(ECD),而超过一半的自身抗体针对所谓的主要免疫原性区域,因此免疫吸附可以作为一种适合MG患者治疗的技术。
数十年来对免疫吸附(immunoadsorption,IA)应用于自身免疫疾病(autoimmune diseases,AID)的研究已经证明这是可行的。然而,由于研究对象数量较少,缺乏随机和对照等,导致结果存在偏差,很难将这种方法推广成标准临床应用。到目前为止,这种治疗还没有产生成本效益,效果并没有优于当前的标准治疗,而且成本更高,程序也更复杂。尽管如此,在更接近临床应用条件下的体内实验,仍可更好地评估免疫吸附(immunoadsorption,IA)治疗潜力。随着对自身免疫疾病病理机制的深入研究,越来越多体外免疫吸附的潜在靶点被确定,选择性免疫吸附被正式用于临床治疗的希望正在快速实现。
参考文献
JI Fang-Ling,WU Jian,JIA Ling-Yun.Research Progress of Immunoadsorption in The Treatment of Autoimmune Diseases: a Review[J].Progress in Biochemistry and Biophysics,2022,49(01):139-148.

 联系我们
联系我们





