
20世纪80年代,一群比利时的学者正在研究水牛昏睡症,项目研究时,一位曾在研究组学习的学生表示可以分析骆驼的血液。该项目的负责人,来自布鲁塞尔自由大学(Vrije Universiteit Brussel)的 Serge Muyldermans同意了这个请求,并在不久之后让学生在锥虫病实验课程中对血液样本中的抗体进行分离。因为担心感染,学生最后用了冰箱剩余的骆驼血液实验。然而学生们在对骆驼血液样本进行实验时,结果却总不符合预期:只能得到抗体重链的分子,而轻链部分却不知所踪。这个结果说明要么学生们的操作有错误,要么来自骆驼血液中的抗体不同寻常。此后,Muyldermans团队花了很长时间来证实骆驼的免疫系统确实能够产生这种没有轻链的天然抗体,并在1993年的《自然》杂志上报导了这一惊人发现,纳米抗体得以首次亮相世界抗体舞台。
这一发现的有趣之处在于,骆驼科动物似乎已经修补了一个已经运行了数百万年的系统。在其它动物(包括人体)中,抗体的重轻链配对所组成的Y形结构可以对抗不同的微生物入侵者。纳米抗体的多样性比传统抗体要少,从进化的角度来看,这类仅有一种链的抗体为什么出现?美国弗雷斯诺加州州立大学的结构生物学家科里·布鲁克斯(Cory Brooks)认为这是一次进化事故,因为这类抗体分子量更小,似乎比常规抗体“更擅长中和病毒”。在Brooks看来,纳米抗体在治疗 Covid-19 等传染病、甚至在所有疾病领域都具有很大潜力。病毒所致的传染病可能是使用纳米抗体治疗的最佳靶标之一,特别是考虑到纳米抗体在骆驼科动物进化中可能扮演着“病毒中和剂”的角色。
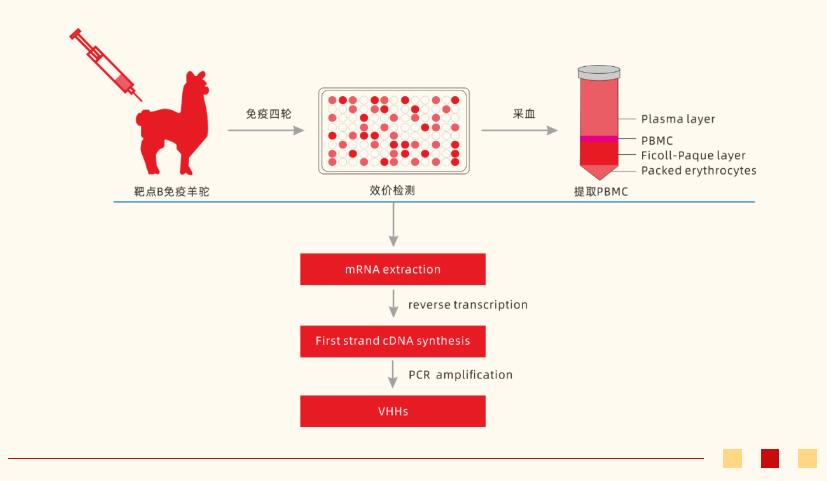
纳米抗体的获得主要通过免疫羊驼由羊驼体内自身的抗体成熟阶段来得到抗体基因,然后通过噬菌体展示筛选技术来从羊驼抗体库中筛选得到最适合的抗体序列。整个流程主要包括羊驼免疫、噬菌体文库构建和抗体筛选三个阶段。
羊驼免疫:每只羊驼可以同时免疫1-5个抗原,每次免疫总的抗原量保持在1-2mg之间,体积在2mL以下,将抗原和佐剂1:1乳化使其形成均匀混合物,4°保存,共进行四轮免疫。
噬菌体文库构建:抽提羊驼淋巴细胞中RNA并反转成cDNA文库,利用特殊设计的引物在cDNA文库中再次进行PCR扩增,得到特异的基因片段。随后将特异的基因片段拼接重组在噬菌体载体上,并转染大肠杆菌,最终完成纳米抗体基因文库的构建。
抗体筛选:将靶点抗原或者带有抗原的物质直接/间接的固定在固体载体上,随后加入噬菌体文库和抗原相互作用。作用一段时间后阳性噬菌体会和抗原结合,用洗涤液洗涤固体载体表面,可以将未结合或非特异结合的噬菌体洗去。随后用强酸或者强碱破坏固体载体上抗原和阳性噬菌体的结合,从而得到阳性噬菌体溶液。一般重复进行2-3轮的筛选即可获得符合开发要求的纳米抗体克隆。
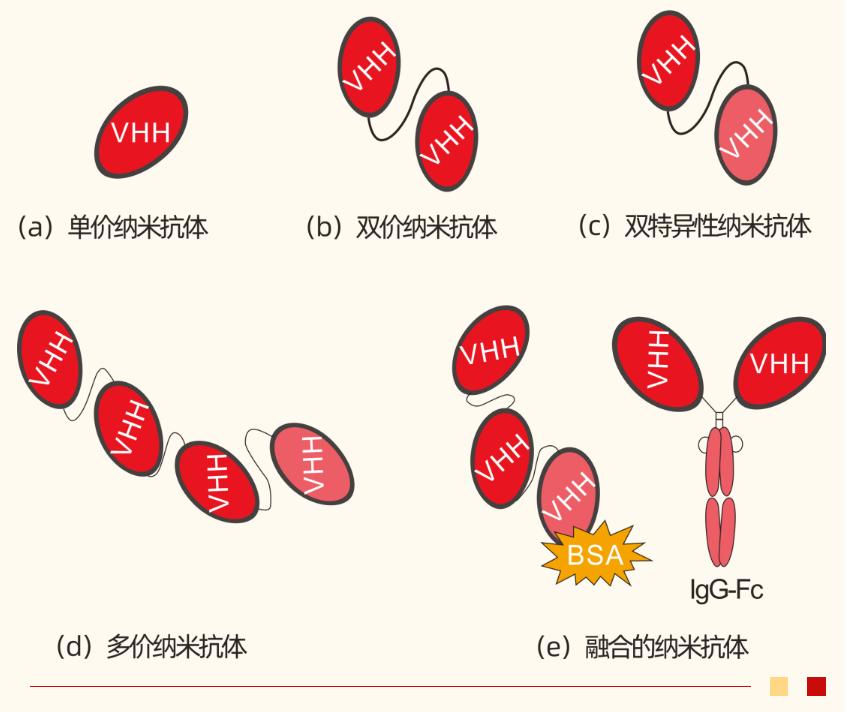
纳米抗体具有分子量小、特异性高等特点。自发现以来,重组VHH已作为科研的基础工具,目前广泛应用于肿瘤学,感染和免疫等医学领域。2018年欧盟批准全球首款用于治疗成年获得性血栓性血小板减少性紫癜的纳米抗体药物—Caplacizumab。2021年康宁杰瑞制药,思路迪医药和先声药业合作开发的PD-L1抗体-恩维达在中国上市,是国内第一个获批上市的纳米抗体药物。2022年获批上市的抗体药物中,日本的ozoralizumab是首次获批的纳米双特异抗体,靶向TNFα/HAS(2+1结构)。
主要应用:
特异性降解细胞内靶蛋白,稳定靶分子构象,进行结构解析;
参与构建多重不同类型的分子结构,连接特定的tag或者荧光蛋白,作为诊断成像工具;
可作为细胞内抗体特异性识别、中和病毒等病原微生物的特殊结构蛋白,提升宿主免疫防御能力;
用于生产双功能抗体或双特异性抗体,增加临床靶向治疗的可能性;
纳米抗体融合蛋白带上酶或者毒素,在组织穿透力、清除速度及稳定性上比普通抗体更有优势,可用于低浓度抗原的检测。
AntibodySystem Magic-XtenNano®Nanobody系列介绍
分子量小:分子量仅15kDa,是传统抗体的1/10大小,空间位阻更小,更易接近靶标
双标签识别:8His+Cys-tag;
高效偶联:独立设计Cys-tag,实现抗体高效定向标记及偶联;
抗体特异性强:对比传统抗体,去掉了FC尾巴,干扰信号更少,背景更低,活性更高
靶点覆盖广泛:2000个活性纳米抗体,近1000个靶点
应用场景广泛:可用于中和阻断、免疫沉淀、免疫印迹、亲和力测定、流式检测、放射免疫分析等相关实验
优秀哺乳表达系统:相比传统纳米抗体大多采用原核表达系统,Magic-XtenNano®Nanobody全系采用法国先进的XtenCHO™哺乳表达系统,能更好的保证抗体正确修饰与活性
质量控制:全系符合欧盟/美国关于抗体质量控制的animal-origin free (AOF)政策,全流程洁净室纯化,内毒含量低,可满足各种实验需求
AntibodySystem Magic-XtenNano®Nanobody热门产品推介:
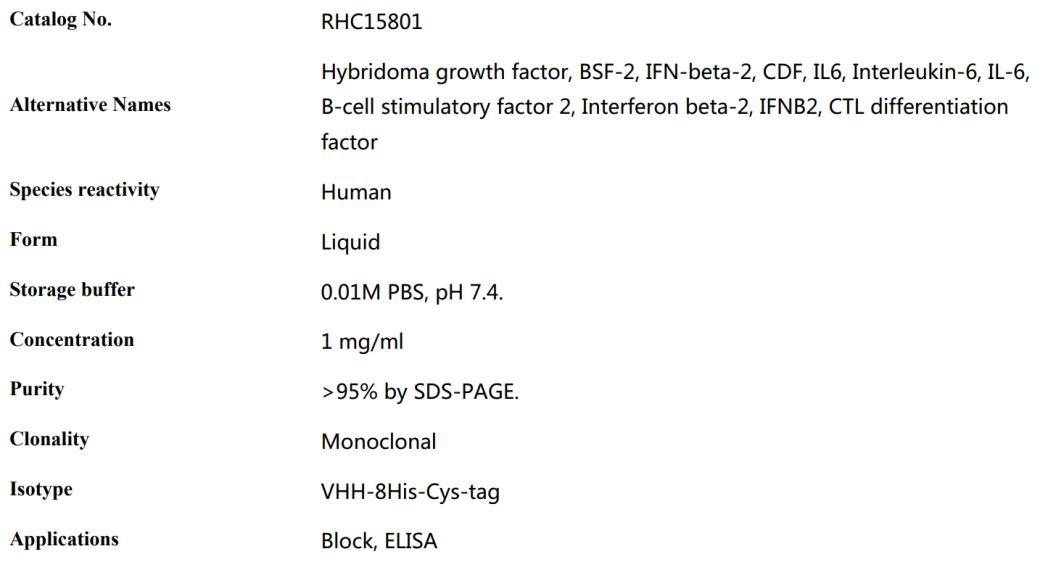
白细胞介素-6(Interleukin- 6),简称白介素6 (IL-6),是一种功能广泛的多效性细胞因子。IL-6可调节多种细胞的生长与分化,具有调节免疫应答、急性期反应及造血功能,并在机体的抗感染免疫反应中起重要作用。IL-6作为抗炎性肌球蛋白的作用是通过其对TNF-α和IL-1的抑制作用以及IL-1ra和IL-10的活化来介导的。
甲状旁腺激素受体1(Parathyroid hormone 1 receptor,PTH1R)是B类GPCRs中重要的一员。PTH1R由PTH的34个N端氨基酸激活,大量存在于骨骼和肾脏细胞中,能与PTH特异性结合后激活下游信号通路,进而调节体内的钙磷代谢。因此,PTH1R被称为钙稳态的中心,是骨质疏松症和甲状旁腺功能减退症的治疗靶点。

MC4R位于基因组第18号染色体,该基因主要在下丘脑神经细胞中表达,是瘦素介导的食欲调节途径中最末端的基因。由阿黑皮素原衍生的α-MSH在下丘脑与其受体MC4R结合,从而产生抑制食欲的生理效应。MC4R可通过作用于中枢阿片-促黑素细胞皮质素原(POMC)神经元、交感节前神经元以及与之相应激动剂相互作用,调控食物摄入和能量消耗,进而改善肥胖。此外,MC4R还可参与胰岛素敏感性及葡萄糖稳态的调控,已成为肥胖及糖尿病治疗的新靶点。

ACKR3,以前称为CXCR7,在B淋巴细胞和T淋巴细胞、神经元和内皮细胞等细胞中表达,并在包括心血管和神经元发育过程以及造血干细胞/祖细胞的迁移和归巢中发挥关键作用。ACKR3最初还因其与趋化因子结合的能力而被称为趋化因子受体。趋化因子是由免疫细胞分泌的小分子蛋白,能够介导免疫反应,在肿瘤的发生和转移中也证实了有趋化因子的参与。ACKR3在各种类型癌细胞以及肿瘤相关的脉管系统中表达,研究表明其与肿瘤生长、转移、以及化疗的耐药性等不良预后相关。

AntibodySystem
更多同系热卖产品
如果您对我们的产品感兴趣,您可以直接扫下方二维码或点击文字链接,实时与我们产品专员沟通!产品咨询电话:027-65279366或者027-87433958


 联系我们
联系我们