很多人不知道,抗体药物研发,最关键的一步是。。。
咨询,问对人很重要![]()
一个双特异性抗体药与普健的故事,四年征程,未完待续。。。
那是风和日丽的一个下午,叮咚~
一条消息跳了出来,“要开发双特异性抗体药物,你们有专家吗?”
“我们的抗体药物专家经验丰富,曾经成功开发过上市治疗性抗体药物,可以针对具体需求进行个性化设计。AtaGenix将全程为您服务。”
随后,一项历时四年的工程由此展开。
目标:开发一种双特异性抗体药物,通过连接CD3抗体,增强针对某类特定肿瘤细胞A的免疫系统识别能力。
要开发双特异性抗体,我们得先分别获得抗单种抗原的鼠单抗---CD3抗体和肿瘤抗原A的抗体。然后进行双特异性抗体设计、表达及纯化,对正确组装后的双抗进行检测,最终实现大规模生产。
路得一步一步走,每一步都很关键。
这就需要我们的单克隆抗体开发技术(点击可查看技术详情)。
已知目标蛋白在哺乳动物表达系统里很难表达,但我们就是解决困难的。
接下来,沿着单克隆抗体开发流程,看一下我们是怎样做到的。
经过预测和评估,我们选择了目标蛋白的一个片段在哺乳动物细胞中进行表达。
虽然,该基因是针对哺乳动物细胞表达而设计和优化的。
但是,我们向来不只做单一准备,永远备有为客户准备的Plan B。So,除了哺乳动物细胞表达系统,我们还选了大肠杆菌作为备用系统。两种表达方案同时进行,最终获得满足条件的抗原。

用原始抗原免疫五只小鼠,并筛选阳性血清。
为了筛选到符合要求的抗体,我们将绿色荧光蛋白GFP与抗原蛋白在哺乳动物细胞中融合表达,通过FITC信号将表达GFP的细胞筛选出来,作为流式分析抗体特异性的阳性细胞;并使用能够识别GFP的一抗作为阳性抗体对照,来筛选特异性抗体。
流式分析检测结果(GFP抗体和GFP阳性细胞百分比):
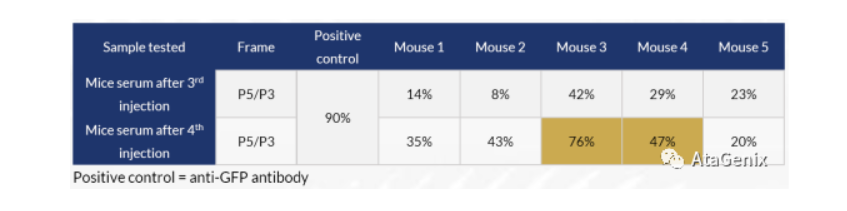
流式检测中对抗原免疫原性最强的为3号小鼠血清,4号次之,我们决定对小鼠3号和4号进行融合。
将筛选出的两只小鼠脾细胞分别进行融合、亚克隆,FC检测保留最佳阳性抗体,最终获得最佳的30株抗肿瘤抗原A候选单克隆抗体杂交瘤细胞株。
看一下我们都做了哪些工作☟
a. 对3号小鼠细胞融合后的上清,进行ELISA检测,从中筛选出42株阳性细胞株(下表)。
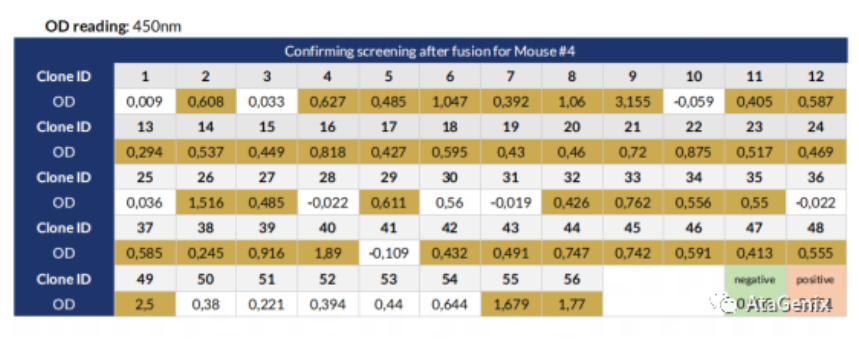
b. 对3号小鼠细胞融合后的上清,进行FC检测,从中筛选出14株阳性细胞株(下表)。
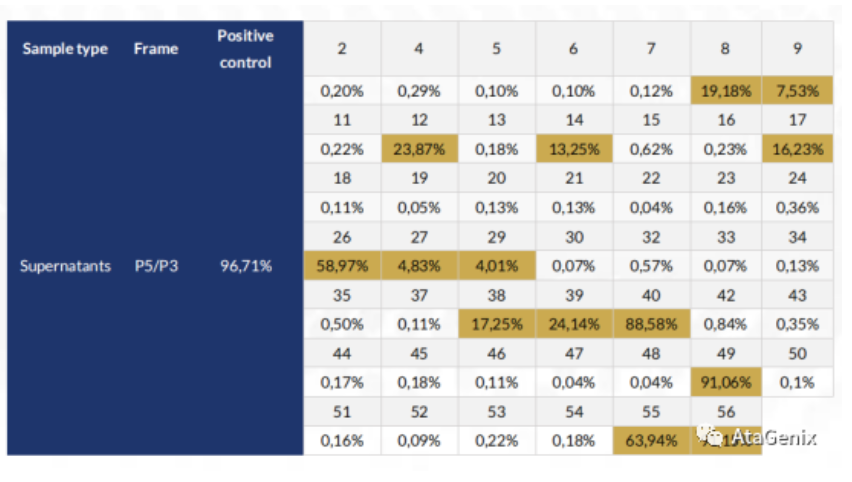
c. 生产的抗体,进行FC检测,从中筛选出30株阳性细胞株(下表)。
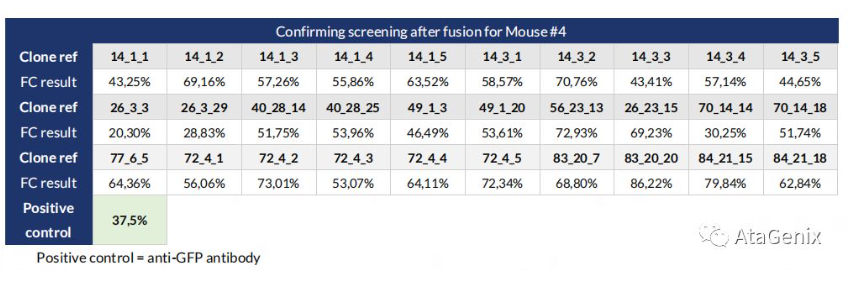
小结
经过多系统表达测试,我们成功地在哺乳动物细胞中重组表达了目标抗原,开发出对抗原具有良好亲和力和特异性的单克隆抗体。最终,我们生产并纯化得到了30株抗肿瘤抗原A抗体的单克隆细胞株,产生的抗体均可以在流式细胞术中成功识别抗原。
抗肿瘤抗原A杂交瘤测序获得鼠单抗的VH和VL序列。
做了8个嵌合抗体的表达纯化,将8个嵌合抗体和1个原始杂交瘤细胞纯化得到的抗体进行ELISA验证,用Biacore检测了这9个抗体的亲和力,筛选到了高亲和力的嵌合抗体。
表达了18个人源化抗体,将18个人源化抗体、原始杂交瘤细胞纯化得到的抗体及筛选得到的最佳嵌合抗体,进行ELISA验证,用Biacore检测了这20个抗体的亲和力,筛选得到高亲和力抗体。
接下来,是最关键的一步。别眨眼哦!
目标:抗肿瘤抗原A和CD3的双特异性抗体
我们已获得3个抗肿瘤抗原A抗体,1个抗CD3抗体。
AB1(前期项目中开发并测序的小鼠杂交瘤单克隆抗体)
AB2和AB3(通过噬菌体展示开发的人源单克隆抗体)
AB4 (AB4h)是在专利中公开的的抗CD3人源化抗体
我们的抗体设计专家设计了3种类型的双特异性抗体,即CrossMAb,IgG-like format using DuoBodies,and IgG-like bivalent Fab-Fab-Fc format。
将cDNA序列亚克隆到AtaGenix特有的哺乳动物细胞表达载体pTXs1中,本项目共使用21个表达质粒(下表):
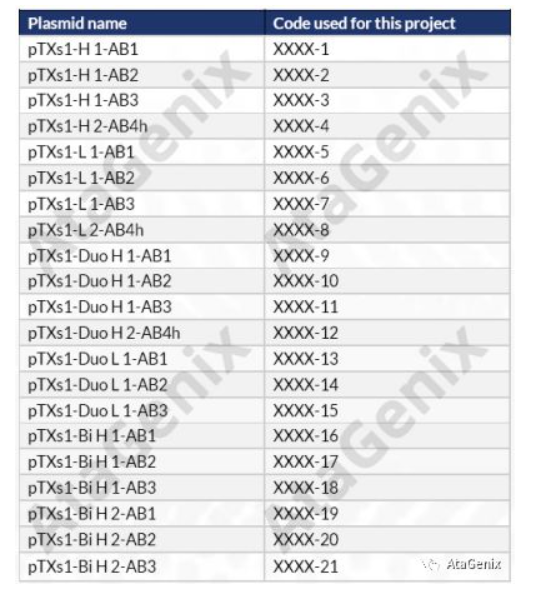
总共16种抗肿瘤抗原A和抗CD3的重组抗体片段用于测试。
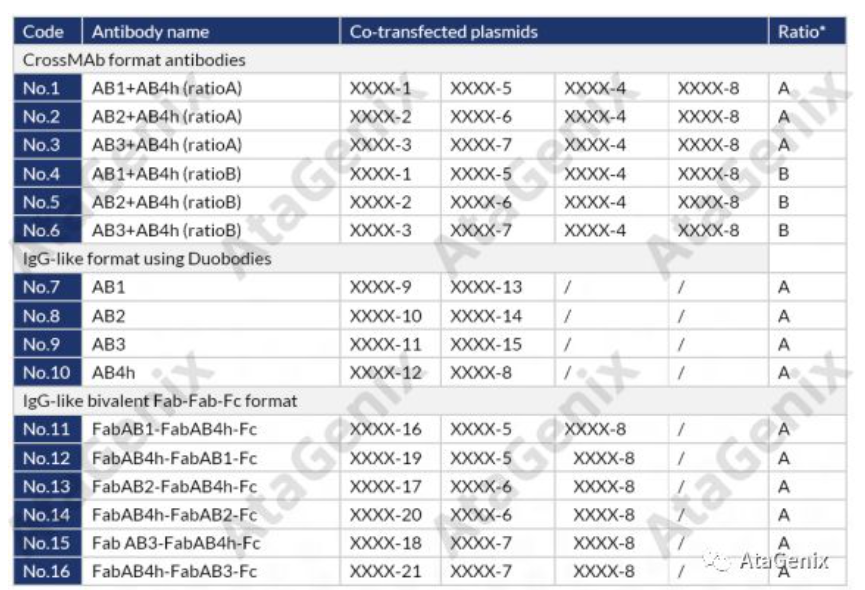
表达测试结果如下:

CrossMAbs类型重组抗体表达纯化测试
结果表明,CrossMAbs是表达的,但没有以完整的双特异性抗体结构组装,处于半形成状态。
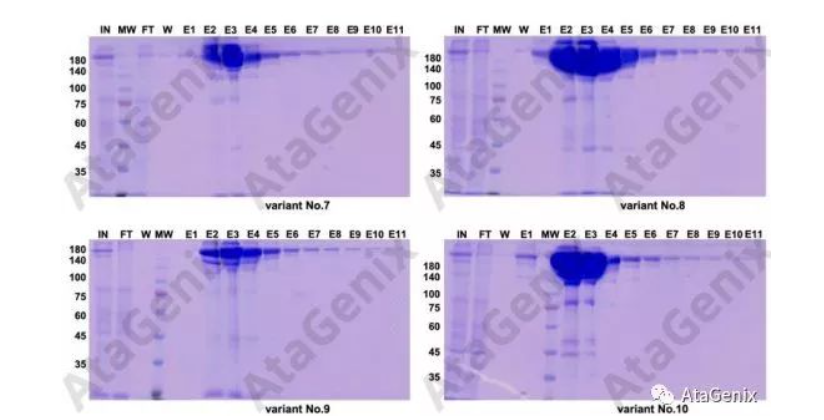
DuoBodies类型重组抗体表达纯化测试
No.7: AB1重组抗体;No.8: AB2重组抗体;No.9: AB3重组抗体;No./10: AB4重组抗体
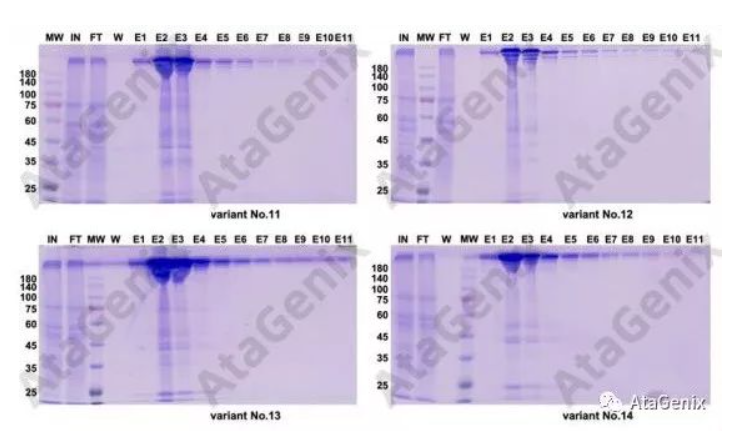
Bivalent Fab-Fab类型重组抗体表达纯化测试

重组抗体QC结果(还原胶和非还原胶)
结果显示,对于DuoBodies和Bivalent Fab-Fab抗体类型,正确地产生了完整的双特异性抗体结构。
值得一提的是,我们整个表达纯化过程对内毒素进行了有效的控制和去除,将内毒素控制在<0.1EU/mg。
上面获得的DuoBodies类型重组抗体,目前只能特异识别单一抗体,如何将两种抗体组合连接,就需要神奇的Fab臂交换技术。
通过特定的条件,进行Fab臂交换重组抗肿瘤抗原A抗体和抗CD3抗体,形成双特异性抗体。
对交换重组的双特异性抗体进行检测:
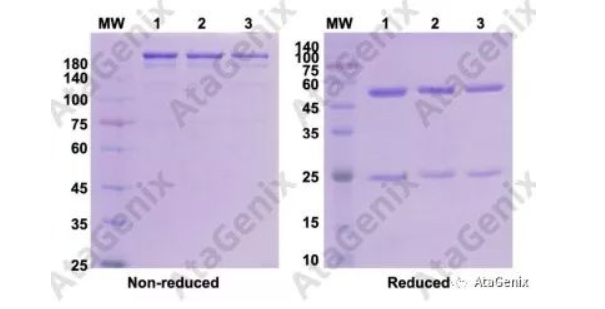
重组DuoBodies抗体QC结果(还原胶和非还原胶)
1:No.7+No./10;2:No.8+No./10;3:No.9+No./10
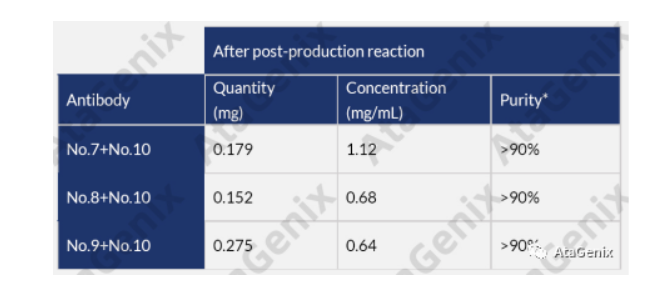
重组DuoBodies抗体产量及纯度
5.1)SEC-HPLC Analysis
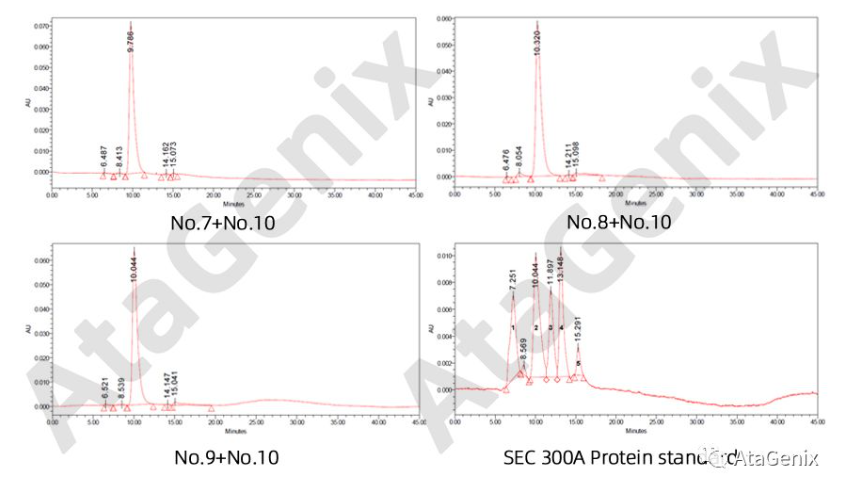
SEC-HPLC检测结果表明,No.7+No./10重组双特异性抗体浓度最高,是由两个重链和两个轻链组成的理想杂合四聚体。No.8+No./10重组抗体有一些降解或未组装完全,No.9+No./10重组抗体显著降解或组装较少。
5.2)ELISA滴定
ELISA滴定法同时测定双特异性抗体和以前获得的亲本抗体(AB1、AB2和AB3)对肿瘤抗原A和CD3的结合能力。
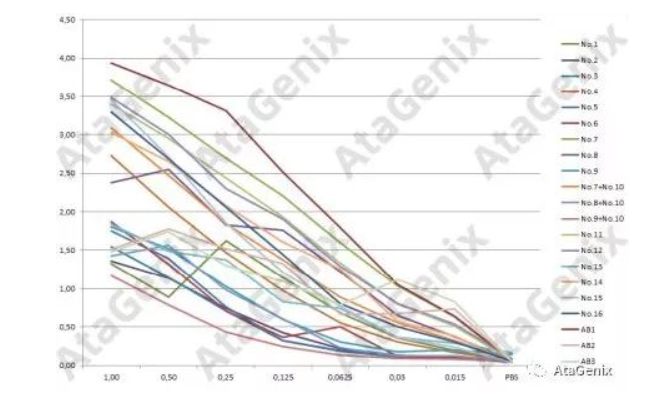
针对肿瘤抗原A结合检测
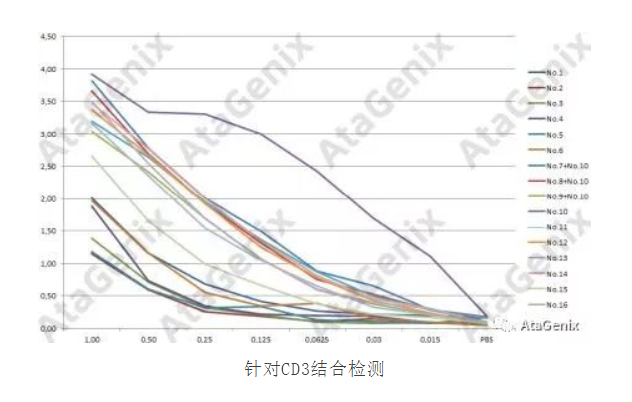
针对CD3结合检测
检测结果显示,所有阳性对照与预期一致。
DuoBodies和Bivalent Fab-Fab抗体与肿瘤抗原A和CD3结合良好,说明这两类重组双特异性抗体构建正确。虽然CrossMAbs类型抗体也会结合,但它们的结合很可能是由半合成状态的抗体造成的。
项目的顺利推动,其中包含2000多封邮件沟通,30多个技术人员辛勤实验,历时4年,中法科学家通力合作。
目前,其中一个双特异性抗体已经完成开发,生产并交付客户1.237g抗体。接下来,客户计划采用我们拥有自主知识产权的细胞株进行稳定细胞株构建,后续事宜正在商定中。

 联系我们
联系我们





