以中国科学院微生物研究所带头的中国科学家首次报告了一种能够有效预防和治疗新型冠状病毒(SARS-CoV-2)及其突变株的抗体。该研究论文《A broadly neutralizing humanized ACE2-targeting antibody againstSARS-CoV-2 variants》在线发表于Nature Communications。

研究人员通过细胞培养和快速筛选,获得靶向多种冠状病毒受体ACE2的阻断抗体,这种抗体经过抗体人源化工程的改造,得到了靶向人ACE2受体的阻断型单克隆抗体h11B11。
新型的人源化抗体h11B11在多种冠状病毒的中和评价中取得良好反馈,在实验中对SARS-CoV、SARS-CoV-2及其突变株病毒均表现出了很好的抑制活性。研究还提到,人源化抗体h11B11与新冠治疗性抗体CB6配合使用可提高中和活性。
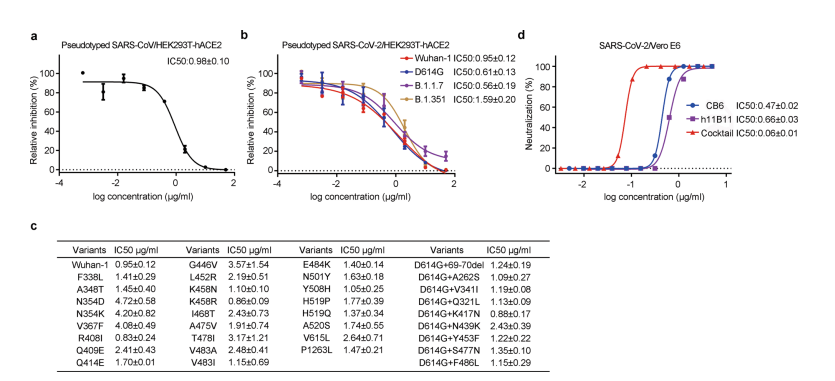
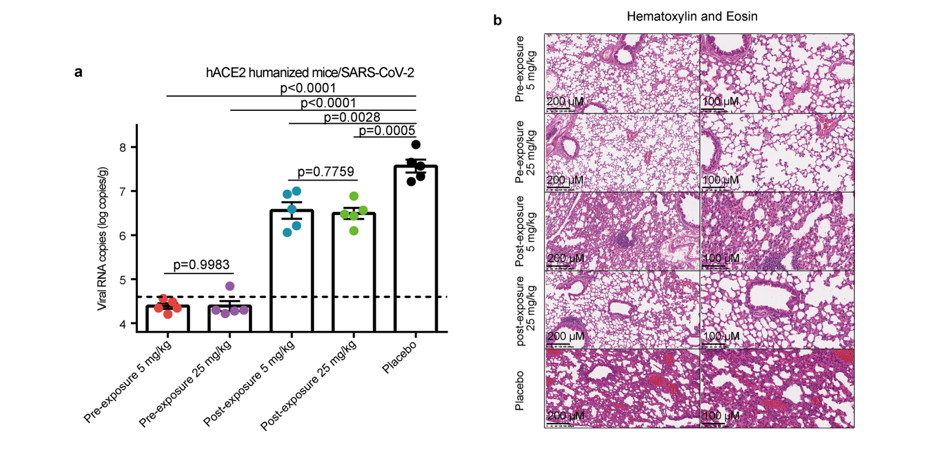
为了进一步探究人源化抗体h11B11的体内活性,研究人员建立了hACE2转基因小鼠感染SARS-CoV-2模型,结果表明,相比于安慰剂组,使用人源化抗体h11B11的进行的预防组小鼠肺部病毒检测量几乎为0,治疗实验组小鼠肺部病毒滴度明显下降。相应组的肺部病理切片结果也与上述检测结果相呼应,表明该人源化抗体在预防和治疗的实验组中有明显改善效果。
ACE2受体在机体内具有维持血压平衡的作用,那么在使用人源化抗体h11B11时,两者结合是否会影响ACE2受体的生理功能呢?
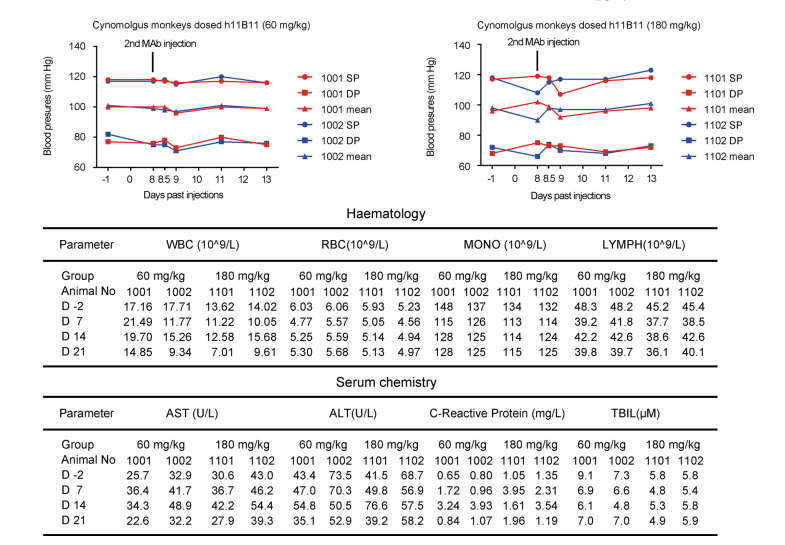
为了验证这项结果,研究人员借助食蟹猴模型对人源化抗体h11B11进行了临床前安全性评价。该模型中,研究人员将4只雄性食蟹猴随机分成2组,分别进行高(180 mg/kg)、低(60 mg/kg)两组剂量的重复给药(每周一次,持续三周),在此过程中对两组食蟹猴的血压和临床病理学改变(血液学和血清生化)进行监测。实验结果表明,在高剂量组的人源化抗体h11B11给药实验中,食蟹猴血压和病理学指标均未发生显著变化,验证了该人源化抗体在体内具有良好安全性。
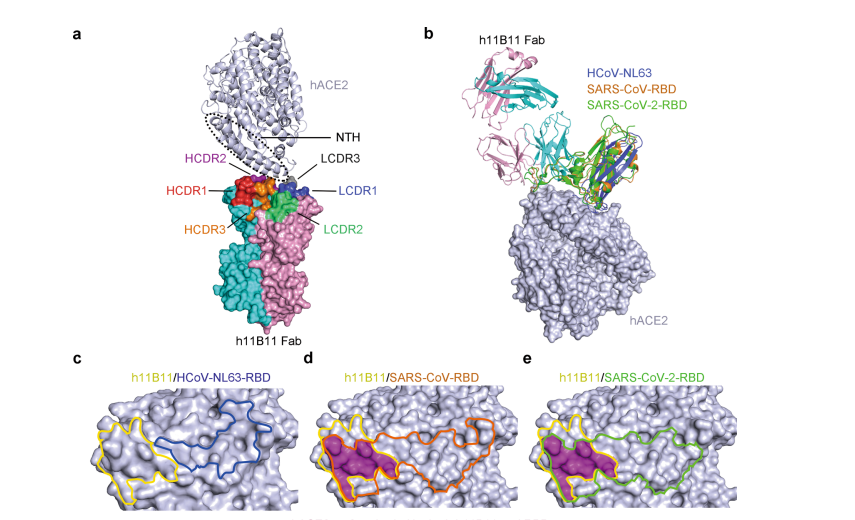
为了进一步明确人源化抗体h11B11的作用机制和结合表位,研究人员对人源化抗体h11B11和受体ACE2的晶体结构进行了解析。根据结构分析,该人源化抗体主要与ACE2受体N端的α螺旋结构域结合,人源化抗体h11B11通过表位竞争和空间位阻效应,通过阻断冠状病毒(SARS-CoV和SARS-CoV-2)RBD与ACE2受体的结合来抑制病毒入侵。
文献参考:
Yanyun Du1,e.t.A broadly neutralizing humanized ACE2-targetingantibody against SARS-CoV-2 variants,https://doi.org/10.1038/s41467-021-25331-x

 联系我们
联系我们





