辉瑞(Pfizer)近日于新英格兰医学期《New England Journal of Medicine》发表呼吸道融合病毒(Respiratory syncytial virus,RSV)疫苗的第三期临床数据,结果显示RSVpreF疫苗可预防60岁以上族群RSV感染相关急性与下呼吸道疾病。

了解呼吸道合胞病毒
人类呼吸道合胞病毒,又称呼吸道融合病毒,简称HRSV(Human Respiratory Syncytial Virus),其名称来源于感染细胞融合时形成的大型细胞,即所谓的合胞体,根据病毒外膜表面的G protein多糖蛋白不同分为A,B两型。
HRSV病毒常爆发于晚春和秋季,有时夏季亦可见,病毒潜伏期(Latent period)约2至8天,病毒脱落期(Shedding period)一般为3至7天,但在幼儿体内可长达2至3周,是世界范围内引起5岁以下儿童急性下呼吸道感染(ALRTI)最重要的病毒病原。
传染途径经由人与人直接接触传染,也会经由接触感染过的体液被传染,因此预防感染应以实施接触隔离为主。
感染后一般伴随发烧咳嗽和呼吸急促,对于患有哮喘基础病、年幼或老年人等免疫系统较弱的群体,HRSV感染可能导致支气管炎、肺炎和中耳炎等重症甚至危及生命。
据统计,每年全球因HRSV引起的呼吸道感染人数约3.31亿,导致约320万5岁以下儿童住院治疗,其中约6万死亡;全球老年人因HRSV住院病例数约33.6万,住院死亡约为1.4万。
HRSV蛋白结构
人类呼吸道合胞病毒(HRSV)是一种单股负链RNA病毒,属于Pneumoviridae科,Orthopneumovirus属。HRSV病毒基因组长度约为15kb,编码了十个基因,其中包括两个表达出单个蛋白质的基因(NS1和NS2),以及八个编码多个蛋白质的基因,包括表面糖蛋白G、F和SH,以及核衣壳蛋白N、P、L、M2-1和M2-2。
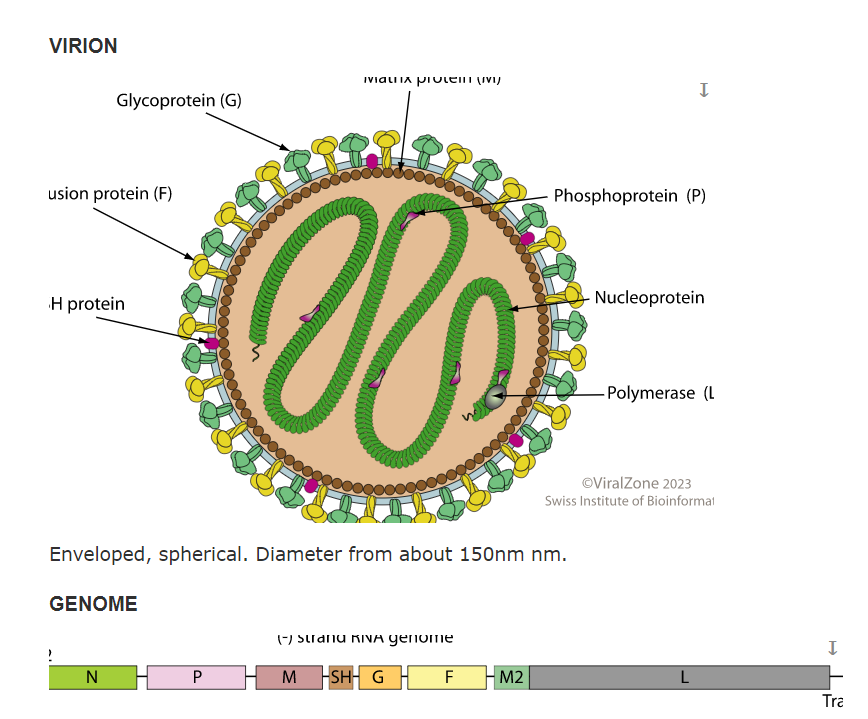
Negative-stranded RNA linear genome, about 15 kb in size. Encodes for 11 proteins
HRSV是一种螺旋状的颗粒,直径为150-300纳米。该颗粒由四种主要结构组成,包括外膜蛋白(F和G)、核衣壳蛋白(N)、RNA聚合酶蛋白(L)和调节蛋白M2-1。外膜蛋白包括F和G,它们在病毒颗粒表面形成三维立体网格结构,是HRSV病毒的主要抗原位点,也是病毒与宿主细胞的相互作用的关键因素。
表面蛋白G(糖蛋白)主要负责病毒与宿主细胞的结合,在不同菌株之间高度变异。
G蛋白以膜结合和分泌两种形式行使作用:膜结合形式通过与宿主细胞表面的糖胺聚糖(GAGs)如肝素硫酸盐结合来负责附着;分泌形式则作为诱饵,与抗原呈递细胞相互作用,抑制抗体介导的中和作用。
G蛋白还包含一个类似于CX3C fractalkine的基序,它能够与纤毛支气管宿主细胞表面的CX3C趋化因子受体1(CX3CR1)结合。这种结合可能会改变细胞趋化作用,并减少感染者肺部免疫细胞的迁移。G蛋白还通过抑制包括TLR4在内的几种Toll样受体的信号转导来改变宿主免疫应答。
表面蛋白F(融合蛋白)负责病毒和宿主细胞膜的融合以及病毒颗粒之间的合胞体形成。它的序列在不同菌株之间高度保守。尽管病毒附着似乎涉及F和G蛋白,但F融合发生的过程与G蛋白无关。
F蛋白存在多种构象形式:在前融合状态(PreF)中,该蛋白以三聚体形式存在,并含有主要抗原位点Ø。Ø在体内是中和抗体的主要靶标。
在与宿主细胞表面的靶标结合后,PreF构象发生变化,Ø消失。这种变化使得蛋白质能够插入宿主细胞膜并导致病毒和宿主细胞膜的融合。最后的构象变化导致蛋白质形成更稳定的形式(后融合,PostF)。
与RSV G蛋白相反,RSV F蛋白还结合并激活Toll样受体4(TLR4),从而启动先天免疫应答和信号转导。
核衣壳蛋白(N)包裹着HRSV病毒的基因组RNA,并帮助维持病毒的完整性。RNA聚合酶蛋白(L)是一个大型蛋白质,负责病毒基因组的复制和转录。调节蛋白M2-1则在RNA聚合酶蛋白(L)的调节下协助HRSV基因组RNA的转录。
HRSV相关的疫苗和药物开发
尽管HRSV的基因组长度相对较小,但该病毒的基因编码了复杂的蛋白质结构。研究人员正在深入研究这些蛋白质之间的相互作用,以了解HRSV的生物学机制和病毒的复制过程。这些研究为开发有效的HRSV疫苗和药物提供了重要的基础。
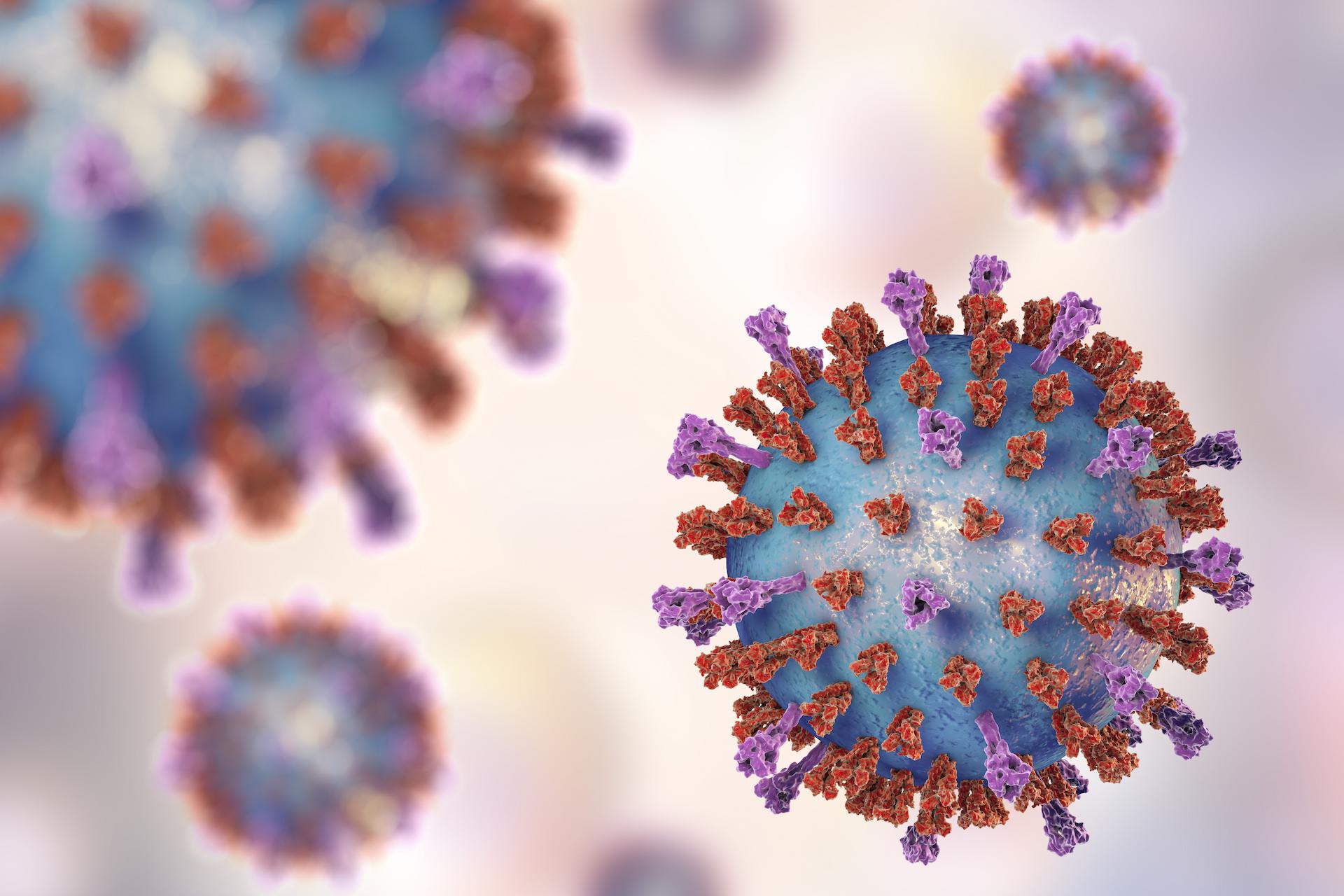
病毒表面的融合蛋白(fusion protein , F)和粘附蛋白(attachment protein, G)因在病毒入侵过程中的关键作用成为病毒研究的理想靶点,而其中G蛋白变异较多相对不稳定,F蛋白也存在Pre到Post构象转变影响其稳定性。
F蛋白是RSV进入宿主细胞时所需的关键跨膜蛋白,它含有多个表位,其中最重要的是A、B和D三个表位。抗体可以与这些表位结合,从而防止病毒的入侵。这些表位和相应的抗体在开发针对RSV的疫苗和药物时具有重要的意义。RSV的G蛋白是一种表面糖蛋白,在人体免疫系统对RSV的反应中,抗体可以与RSV的G蛋白表位GA和GB结合。其中,GA是RSV G蛋白的主要表位。GA表位的抗体可以通过中和病毒或促进宿主的免疫系统清除病毒。需要注意的是,尽管G蛋白是RSV的重要表位,但由于其高度变异性,因此相应的抗体的保护效果相对较低,不如针对F蛋白的抗体强。因此,在研发RSV的疫苗和药物时,主要的目标还是针对F蛋白的表位。
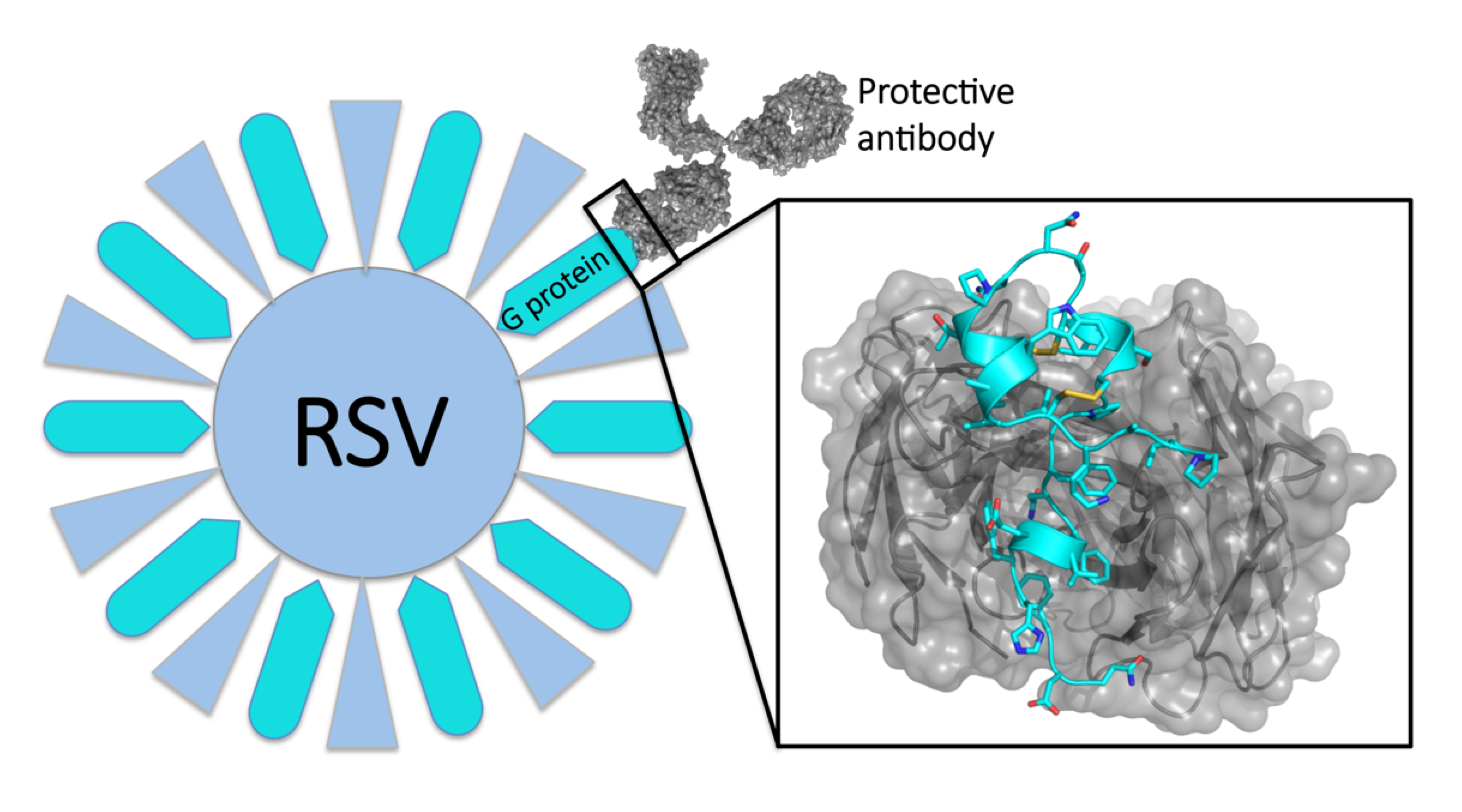
研究人员已经成功地开发出一些与病毒颗粒表面的F蛋白结合的中和活性抗体,这些抗体可能成为新型HRSV疫苗和药物的重要组成部分。除了中和抗体,HRSV病毒的其他蛋白质也被研究人员用作药物和疫苗开发的靶点。例如,HRSV的表面糖蛋白G已被发现具有免疫原性,且其抗原性的片段可用于开发疫苗。此外,研究人员还在探索一些新型的治疗方法,例如RNA干扰和免疫调节剂等。HRSV是一种致命的呼吸道病毒,能够引起包括婴儿、幼儿和老年人在内的人群中的严重疾病,了解其基因信息和病毒颗粒结构对于我们理解其生物学机制和开发有效的疫苗和药物是至关重要的。
普健生物联合法国ProteoGenix科学团队,长期对一系列病毒蛋白展开追踪研究。
案例展示
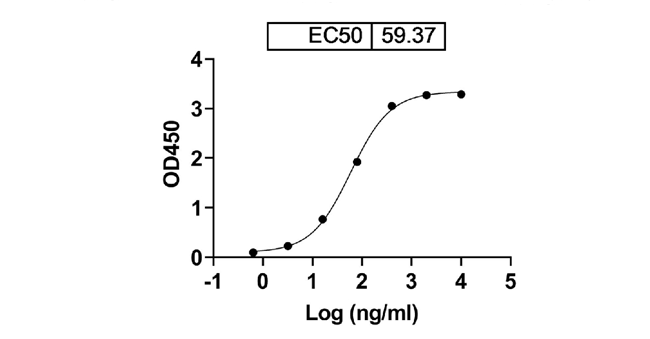
Anti-RSV F protein [MEDI-493] binds with F/Fusion glycoprotein F0
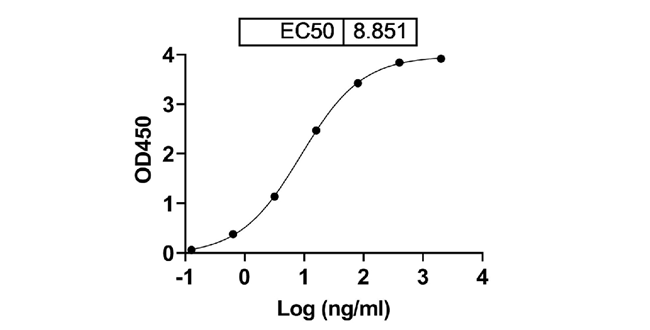
Anti-RSV F Recombinant Antibody (clone MEDI8897)
binds with F/Fusion glycoprotein F0
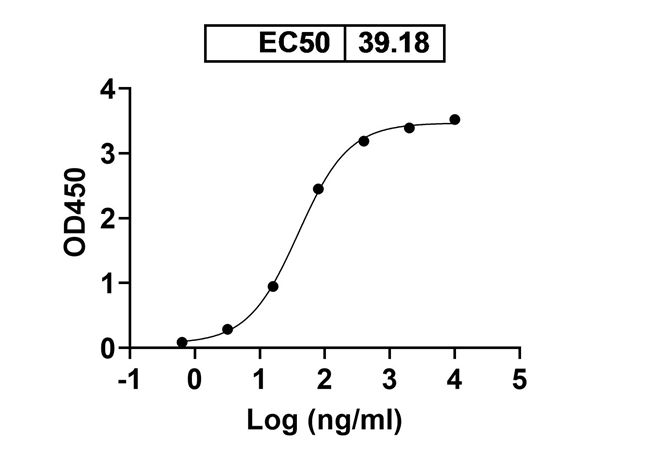
Anti-HRSV F/Fusion glycoprotein F0
Antibody(Am14) binds with glycoprotein F0
RSV疫苗的研发已经有数十年,辉瑞、葛兰素史克和莫德纳近年在研发疫苗取得了很大进展。辉瑞(Pfizer)公司2021年7月底宣布计划在两个月内开始对成人呼吸道合胞病毒疫苗进行3期试验,并于2022年初完成。2021年8月,莫德纳的人类呼吸道合胞病毒疫苗 (mRNA-1345)获得美国食品药品监督管理局(FDA)快速通道指定(Fast track (FDA))。直到今年年初,困扰科学界及各大疫苗研发公司近六十年的RSV疫苗才尘埃落定,辉瑞、葛兰素史克研发的RSV疫苗获得FDA疫苗与相关生物制品产品咨询委员会支持并预计将于5月份获批上市。4月11日,Moderna也将在本季度申请上市其研究性RSV候选疫苗:mRNA-1345。因此2023年将是RSV疫苗商业化元年,百亿市场争夺战一触即发!

 联系我们
联系我们





