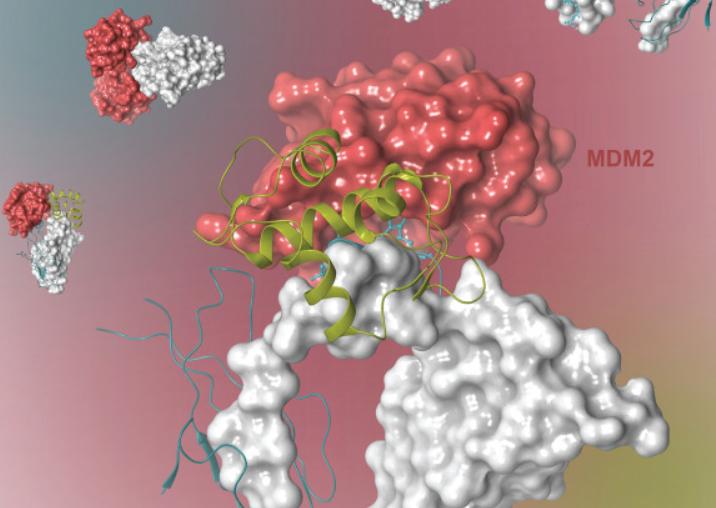
用于嵌合抗原受体(CAR)T细胞治疗的T淋巴细胞也已配备有纳米抗体(Nbs)。表达源自抗体的重组受体的工程化T细胞的过继转移为现代癌症治疗提供了巨大的机会。scFV碎片是最常用的抗原识别模块重组受体。然而,在I期临床试验中,应用基于scfv的治疗性T细胞常导致严重的免疫反应和CAR重定向T细胞在体内的持久性差。此外,由于实体瘤缺乏癌症特异性靶点,因此CAR-T细胞疗法治疗实体瘤的成功率相对较低,但CAR-T细胞疗法已被证明对血液系统癌症有效。由于其固有的低免疫原性,纳米抗体(Nbs)是一种理想的替代重组CAR。Xie等人开发了基于纳米抗体的靶向肿瘤微环境的CAR - T细胞,从而抑制了免疫功能正常小鼠实体瘤的生长。研究表明,PD-L1特异性纳米抗体(Nbs)以及基质和细胞外基质特异性纳米抗体(Nbs)均可将工程T细胞特异性靶向到肿瘤微环境中,从而提高不同肿瘤模型的生存率。这些有前景的结果证明了基于B细胞的CAR-T细胞通过靶向肿瘤微环境治疗实体瘤的可行性和有效性。
此外,纳米抗体(Nbs)还证明了其克服癌细胞抗原逃逸的潜力,这是CAR - T细胞治疗失败的主要原因。为了克服这一局限性,Munter及其同事最近发表了一项研究,在这项研究中,表达双特异性基于纳米抗体(Nbs)的CAR- T细胞能够在体外杀死表达CD20、HER2或两者的肿瘤细胞。结果表明,由两种不同纳米抗体(Nbs)组成的双特异性CAR在工程T细胞的细胞膜上稳定高水平表达。此外,与原始纳米抗体(Nbs)相比,双特异性CAR保留了相似的抗原结合亲和力。然而,未发现这些双特异性CAR在癌症治疗方面有相加或协同作用。这一结果表明,进一步的优化对于实现双价和双特异性Nbs- Car T细胞疗法的充分利用至关重要。
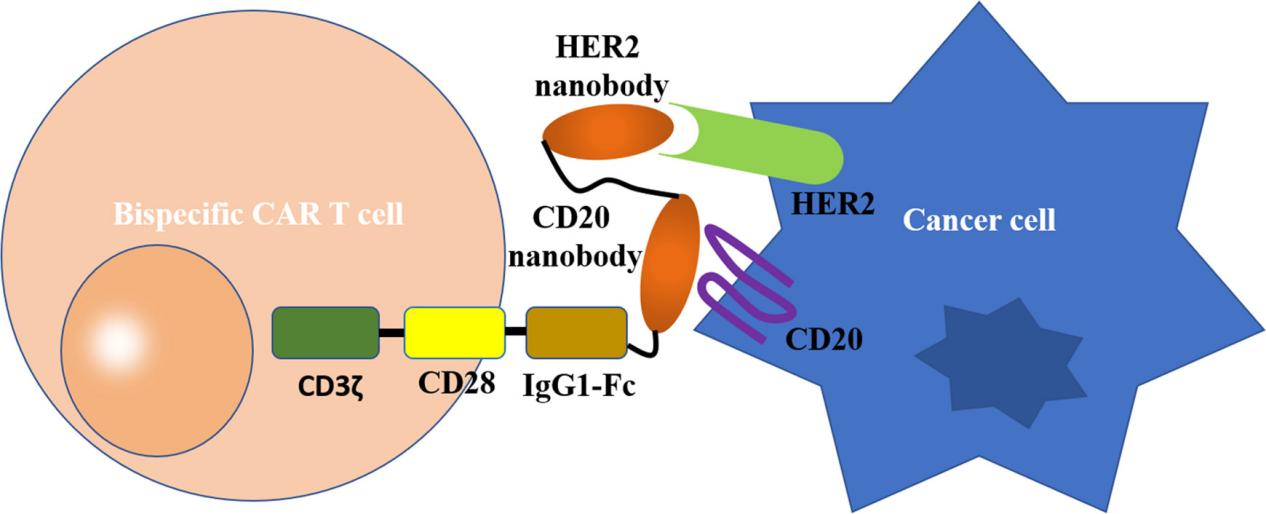
图:靶向癌细胞的双特异性CAR-T细胞。CAR-T细胞中传统使用的抗原识别模块ScFv被分别靶向HER2和CD20的纳米抗体串联取代。CD3ζ, CD3ζ胞内信号域;CD28, CD28跨膜结构域;IgG1-Fc,人IgG1 CH2CH3 (Fc)间隔体。
纳米抗体偶联物已经展示了它们在癌症诊断和治疗中的潜力,其中一些最成功的偶联物已经进入了临床前或临床试验。然而,要实现这些超常规粘结剂的充分利用,还有诸如半衰期、免疫成本、生物安全等问题有待解决。

 联系我们
联系我们





