上篇我们讨论了自噬在B2细胞发育中的作用,本篇我们将继续讨论B细胞代谢及活化B细胞的自噬。
初始B细胞在静止状态下生存,但进入激活状态后会发生怎样的变化呢?
在外周,初始B细胞维持在代谢静止状态,这可能促进其长期生存。然而,当B细胞被激活时,它们的代谢状态迅速被逆转,从而促进生长和增殖。在B细胞活化期间,通过BCR刺激增加线粒体质量和pi3k依赖性葡萄糖摄取,使葡萄糖输入增加。但人类B细胞表达的Glut1相对较少,可能依赖于其他转运蛋白。最近一项研究结合RNA测序和稳定同位素示踪的分析结果显示,在B细胞激活期间,线粒体代谢上调,而非糖酵解。虽然葡萄糖确实通过糖酵途经流动,但大部分转向磷酸戊糖途径,为核苷酸合成和氧化应激管理提供底物。当过度的氧化应激损害细胞活力时,活性氧簇是B细胞中重要的信号分子。除了供给磷酸戊糖途径外,进口葡萄糖还用于从头脂肪生成。代谢决定了B细胞活化后检查点的功能,这一过程中脂肪酸氧化也扮演着重要角色。
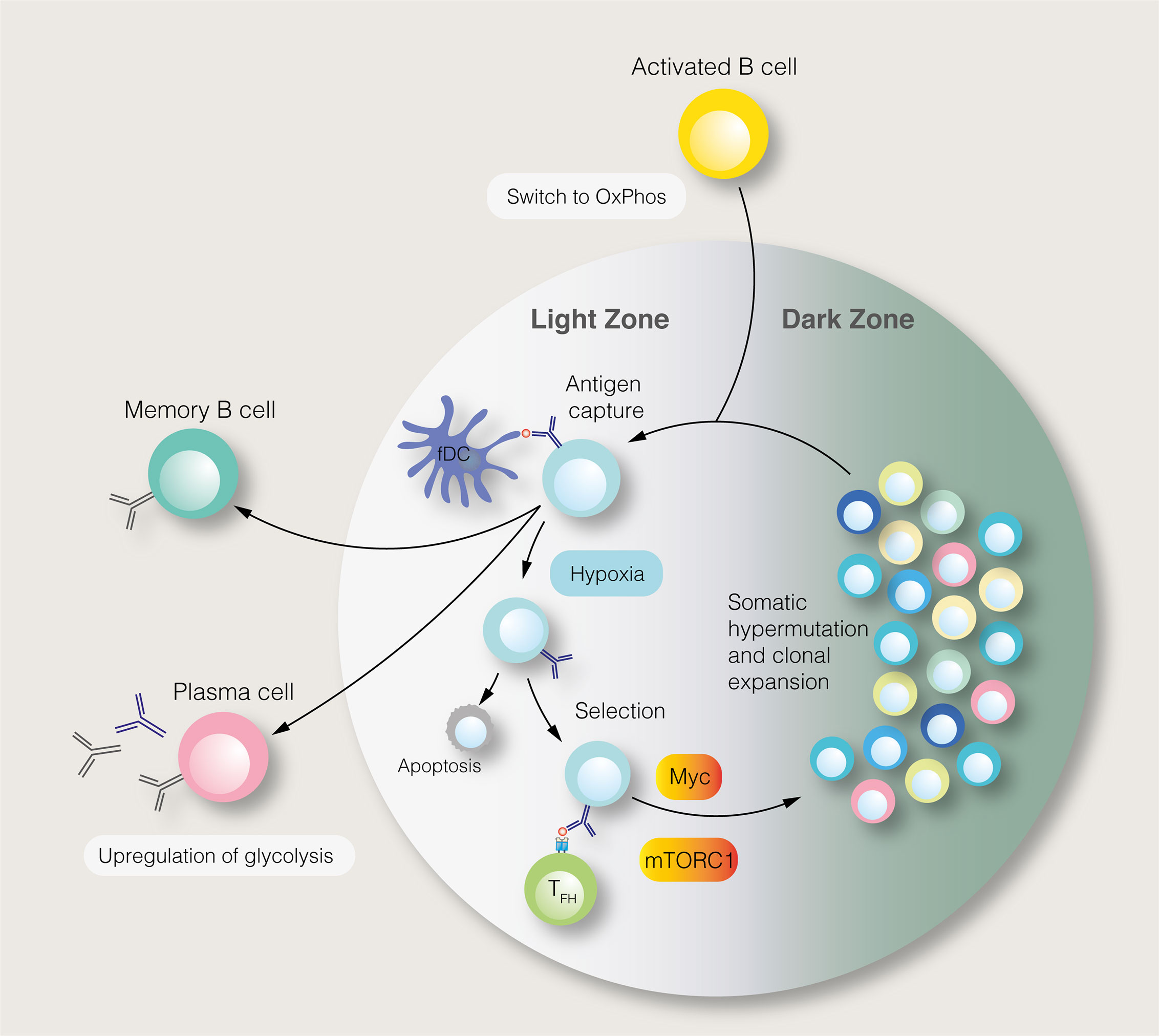
细胞需要经历哪些过程才能产生抗体呢?
首先,B细胞活化后,通过PC分化产生抗体分泌细胞。PC分化过程中,转录因子Blimp1和Xbp1介导内质网扩张。然而,高水平的免疫球蛋白产生导致错误折叠蛋白的积累和内质网应激。为了维持代谢稳态,PC利用了抗氧化反应和未折叠蛋白反应,后者限制了mRNA的翻译,同时增强了蛋白质折叠能力和ER降解错误折叠蛋白的能力。虽然Xbp1和Blimp1控制PC中的UPR,但mTORC1介导预测性UPR,这先于抗体的分泌。错误折叠的蛋白质也通过蛋白酶体降解。令人惊讶的是,在小鼠PC分化过程中,蛋白酶体的能力逐渐下降,蛋白酶体抑制降低了PC的活力。虽然短寿命PC和长寿命PC中表达的内质网应激反应基因相同,但过度的内质网应激被认为是限制短寿命PC寿命的一个因素。

自噬在B细胞活化后的功能中占据着重要的地位,对B细胞呈递抗原的能力有何影响?
在B细胞活化的初始阶段,BCR和T细胞的共刺激对自噬进行差异调节,从而创建自身免疫检查点。某些情况下,B细胞通过自噬来呈递MHC-II抗原,但自噬对浆母细胞分化的影响程度不一。一些早期研究表明,在药物抑制自噬或通过饥饿诱导自噬后,B细胞提呈MHC-II抗原的能力发生了改变。然而,这些研究是在EBV感染的B细胞中进行的,EBV感染改变了B细胞抗原呈递,因此这些结果并不完全适用于生理相关性的研究。最近的研究表明,自噬与BCR结合后的内吞抗原极化有关,从而影响B细胞呈递抗原的能力。在没有自噬的情况下,部分抗原- BCR复合物与含MHC-II的囊泡的共定位被破坏,尤其是颗粒抗原的情况下。
自噬在GC反应中发挥重要作用,还能影响我们的免疫应答。
GC反应能够产生记忆B细胞和LLPCs,其特征也是广泛的B细胞自噬。自噬在代谢稳态和错误折叠蛋白降解中的作用,似乎在SLPCs和LLPCs的抗体应答维持中发挥重要作用。然而,其抑制作用的确切效果存在争议,不同的研究显示自噬在抗体产生中的必要性也有所不同。有些研究显示Atg7缺失会影响IgM的短期生成,而有些研究却显示缺乏Atg5的B细胞在LPS刺激后短期抗体生成增加。自噬可能抑制短期免疫球蛋白输出的观点提示,它反而促进了PC的长期活力。在B细胞自噬缺陷的小鼠中,对一些抗原的体液免疫应答降低,LLPC的长期存活率也降低。另一份报告也有相似的发现,并进一步指出自噬对小鼠抗TD抗原卵清蛋白的抗原特异性IgM反应起重要作用。
自噬是延长寿命的关键,LLPCs利用自噬的程度比SLPCs更大,那么自噬是如何影响PC的呢?
在成人骨髓PC中,LLPC中的自噬相关基因表达和自噬发生率的LC3B-II高于SLPC,与人类数据一致,自噬小体在寿命较长的小鼠PC中也更为普遍。自噬似乎在支持小鼠记忆B细胞的长期存活,从而促进免疫记忆的维持中发挥重要作用。记忆性B细胞中自噬相关基因的表达高于其他B细胞亚群,提示自噬相关基因在其功能中发挥重要作用。在B细胞自噬缺陷的小鼠中,针对NP-KLH的继发性体液免疫反应受到的影响远远大于初次免疫反应,表明B细胞记忆功能受损。在缺乏B细胞自噬的小鼠中,免疫后两周形成的记忆细胞数量是正常的,但在免疫后8周,它们的数量明显减少,表明自噬不是记忆B细胞形成所必需的,而是维持记忆B细胞数量所必需的。
参考文献
Iwan G. A. Raza,B Cell Metabolism and Autophagy in Autoimmunity,Front. Immunol., 07 June 2021,Sec. Autoimmune and Autoinflammatory Disorders,Volume 12 - 2021

 联系我们
联系我们





